

Дослідження кристалічної будови органічних сполук і лікарських субстанцій, поліморфізму, фазових переходів та супрамолекулярної організації.
1. Вивичення поліморфізму у кристалах речовин, які проявляють біологічну активність
Поліморфізм у кристалах біологічно активних сполук є одним з ключових напрямків роботи відділу. Зокрема, йому була присвячена робота, виконана за рахунок гранту НФДУ. Відомо, що різні поліморфні модифікації твердих форм лікарських речовин можуть мати принципово різну активність, яка зрештою залежить від кристалічної організації молекул, тому моніторинг і передбачення поліморфізму актуальних та потенційних лікарських засобів є надзвичайно важливим для процесів розробки і виробництва лікарських препаратів.
Одним з яскравих прикладів є відомий препарат пірацетам, який має п'ять поліморфних модифікацій. Попри популярність препарату, в тому числі з точки зору досліджень, наразі причини переходу між формами та їх відносної стабільності були неочевидні. Проведене дослідження кристалічних структур поліморфних модифікацій методами енергетичних векторних діаграм, розробленими та впровадженими у відділі, виявило подібність і водночас суттєві відмінності між ІІ та V модифікаціями пірацетаму, перехід між якими обумовлений дією тиску (Рис. 1):
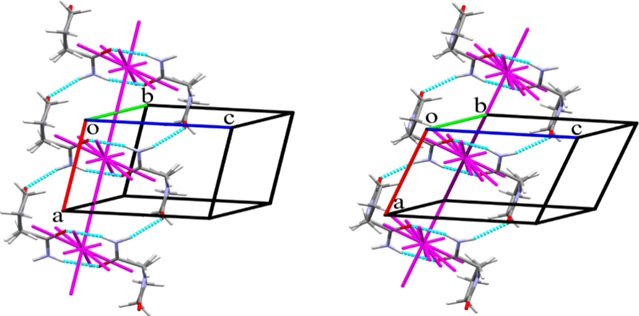
Обидві структури мають близьку енергетичну будову, втім форма ІІ виявляє більшу енергетичну анізотропію (шарувата структура), в той час як у формі V енергія міжмолекулярних взаємодій розподілена більш рівномірно (структура ближча до колончастої). Перехід між цими структурами може бути спровокований зміщенням уздовж певних кристалографічних напрямків без руйнування кристалічної структури; енергетичні параметри цього зміщення були оцінені розрахунковими квантово-хімічними методами (Рис. 2).
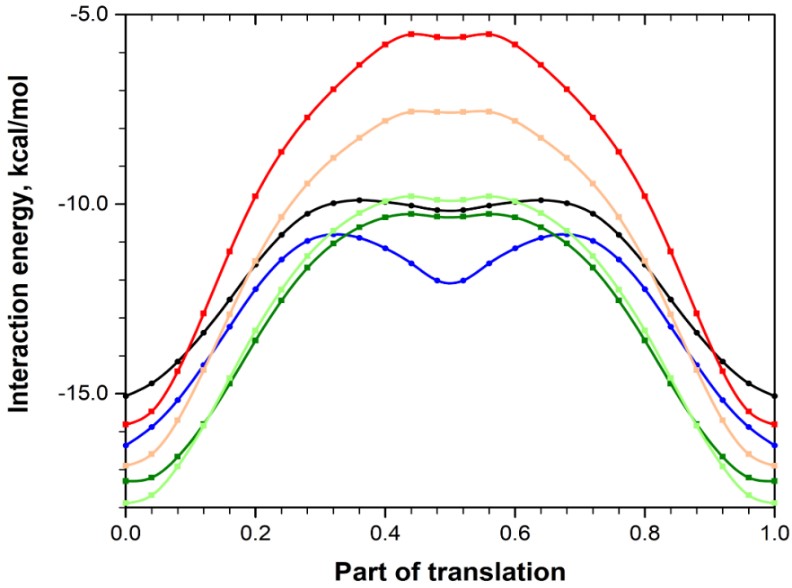
Наявність вторинного мінімуму на кривій енергетичного профілю поліморфів вказує на легкий зсув димерної будівельної одиниці обох кристалів уздовж базового шару, що є передумовою поліморфного переходу між формами. Енергетичні бар’єри зсуву виявились малими та цілком доступними за невеликих значень тиску – наприклад, таких, які досягаються під час механічної обробки речовин на фармацевтичних виробництвах.
Іншим прикладом лікарської сполуки з різними відомими поліморфними модифікаціями може послугувати ібупрофен: він має одну стабільну кристалічну форму, водночас відома друга (нестабільна) поліморфна модифікація та нестабільна аморфна тверда форма речовин. Для вивчення цього кейсу була застосований аналіз конформаційного простору індивідуальної молекули зі скануванням по торсійним кутам, який виявив значні можливості для вільного обертання деяких груп, що є передумовою зміни конформації і, відповідно, кристалічної організації під тиском. Водночас відомі експериментальні дослідження показали, що торсійні кути незначно різняться у різних поліморфних модифікаціях. Моделювання деформації зсуву показало відсутність локальних мінімумів на енергетичному профілі, аналогічних до таких у пірацетамі, та суттєво вищі енергії зсуву, що ж підгрунтям для пояснення експериментальних даних щодо кількості поліморфних модифікацій речовин та можливості переходу між ними під тиском.
Прикладом сполуки, яка може змінювати біологічну активність під час маніпуляцій із фармацевтичною субстанцією, є анальгетичний препарат 1-Аліл-4-гідрокси-2,2-діоксо-N-(4-метоксифеніл)-1Н-2λ6,1-бензтиазин-3-карбоксамід – аналог піроксикаму зі схожею молекулярною будовою. Було проаналізовано будову двох поліморфних модифікацій сполуки та ключові міжмолекулярні взаємодії: результати аналізу методом енергетичних векторних діаграм виявили принципову різницю у будові (Рис. 3)
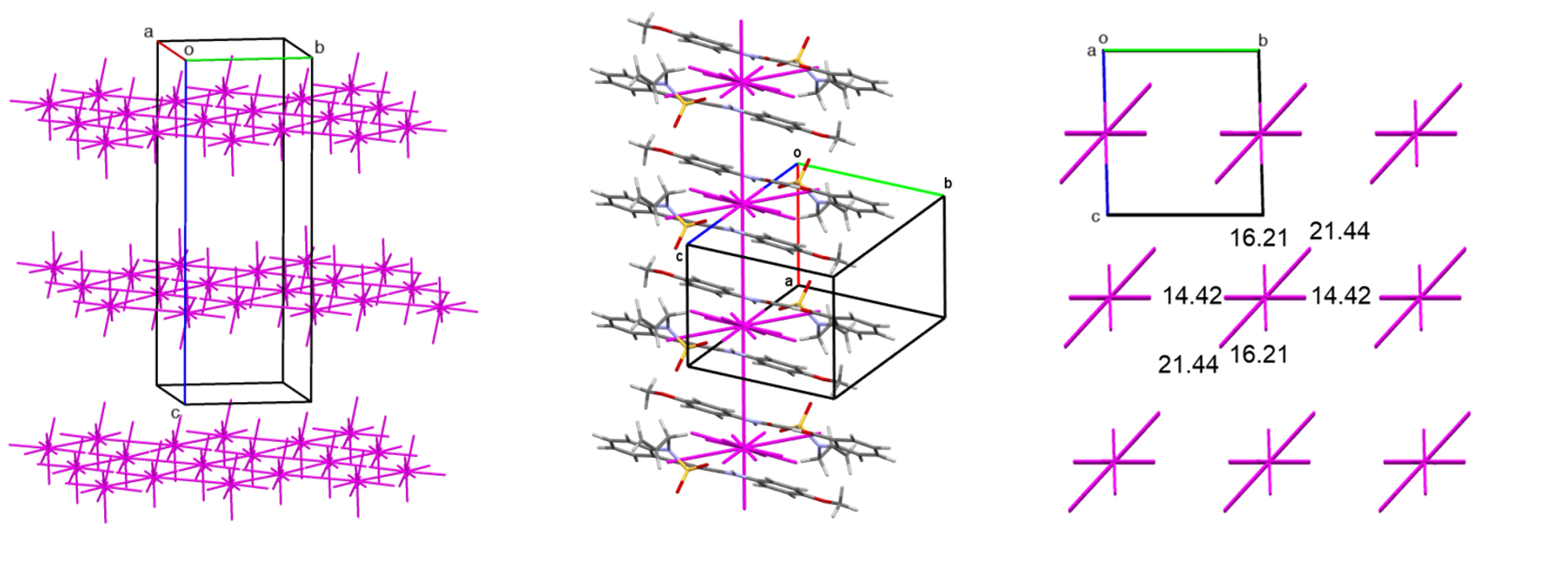
Дослідження методом порошкового рентгеноструктурного аналізу виявило, що обидва поліморфи стабільні за нормальних умов протягом довгого часу, втім спостерігається перехід шаруватої структури у стовпчасту під час розтирання у кюветі (Рис. 4).
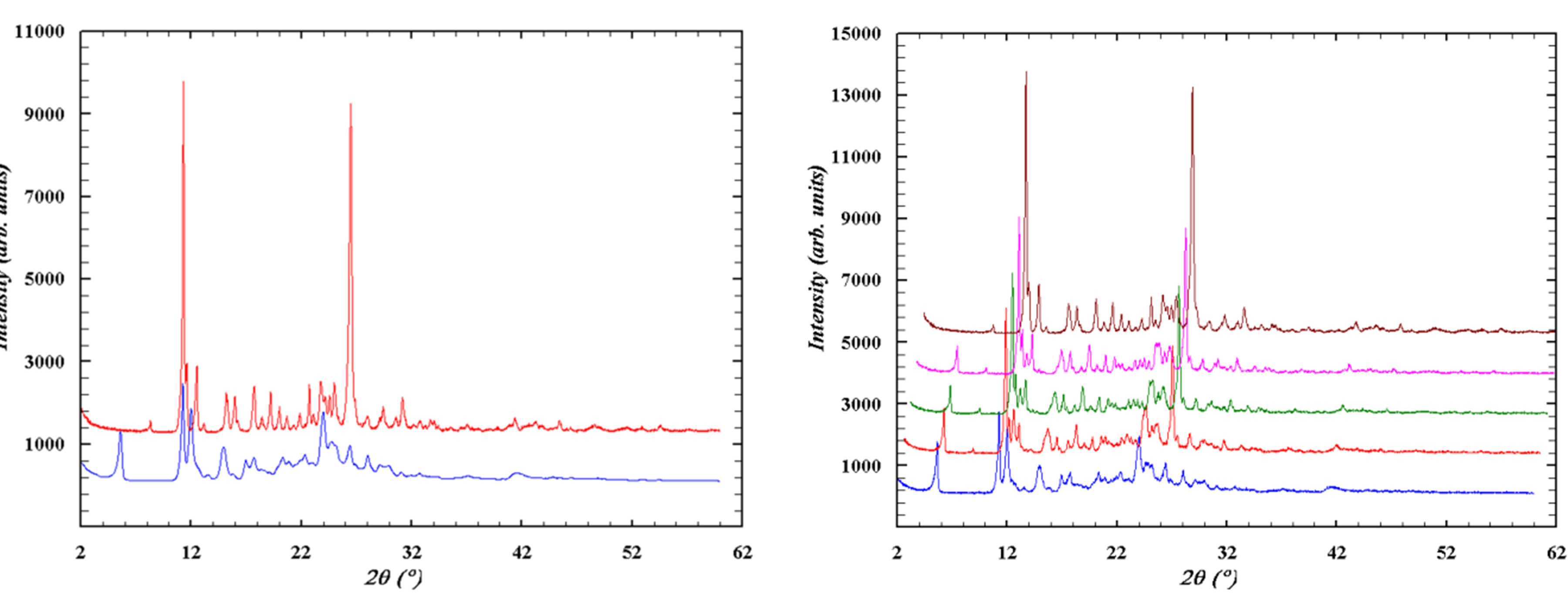
Аналогічна ситуація спостерігається під час механічного впливу на потенційну біологічно активну речовину з ряду оксазолів (3-(1-(трет-бутоксикарбоніл)азетидин-3-іл)-1,2-оксазол-4-карбонова кислота). Комплексні дослідження сполуки методами монокристального та порошкового рентгеноструктурного аналізу, а також квантово-хімічними методами аналізу міжмолекулярних зв’язків дозволили виявити і описати поліморфний перехід між структурами при розтиранні – механічному навантаженні, аналогічному подрібненню при таблетуванні на фармацевтичному виробництві (Рис. 5, 6).
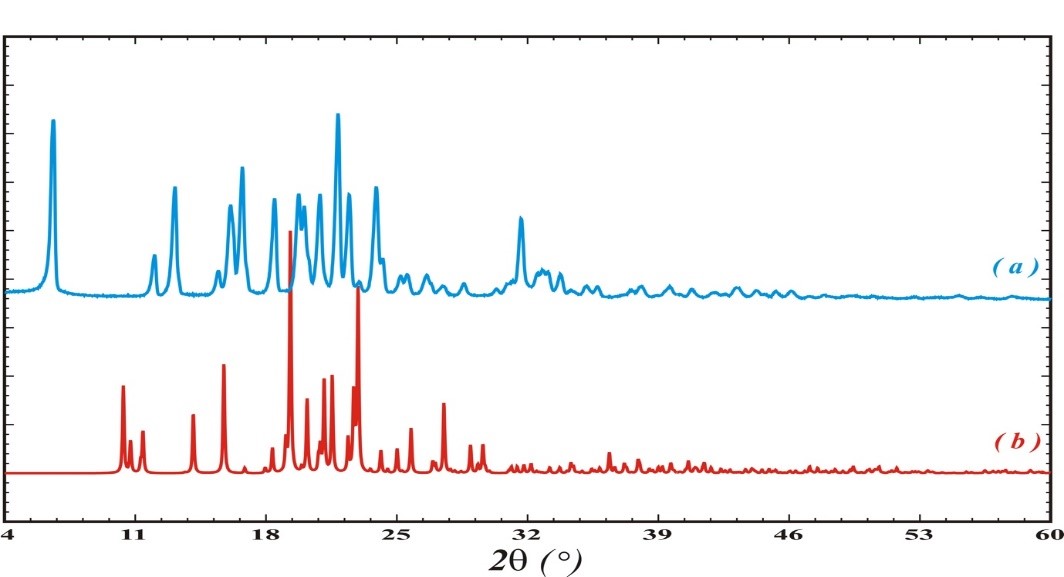
Структура b має стовпчасту структуру (Рис. 6, зліва), в той час як структура а, яка утворюється після розтирання, основана на шаруватій упаковці центросиметричних димерів як основного базового мотиву (Рис. 6, справа).
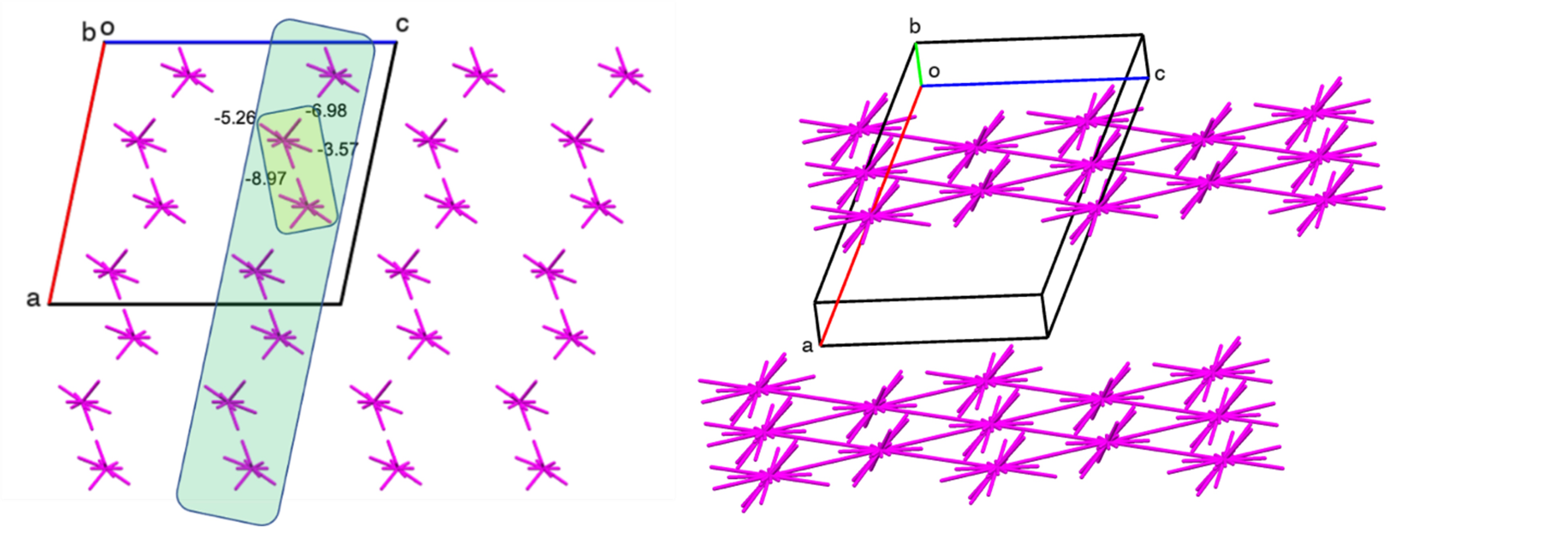
Біологічно активна речовина теофілін також демострує різномаїття різних поліморфних модифікацій. Були досліджені кристалічні структури трьох відомих модифікацій, а також моногідрату та кокристалу сполуки з йодом. Всі поліморфні модифікації є варіантами стовпчасто-шаруватих структур (енергетичні векторні діаграми наведені на Рис. 7), втім із суттєвою різницею, яка полягає здебільшого у ступеню складчастості цих стовпчиків та їхньому взаємному розташуванні.
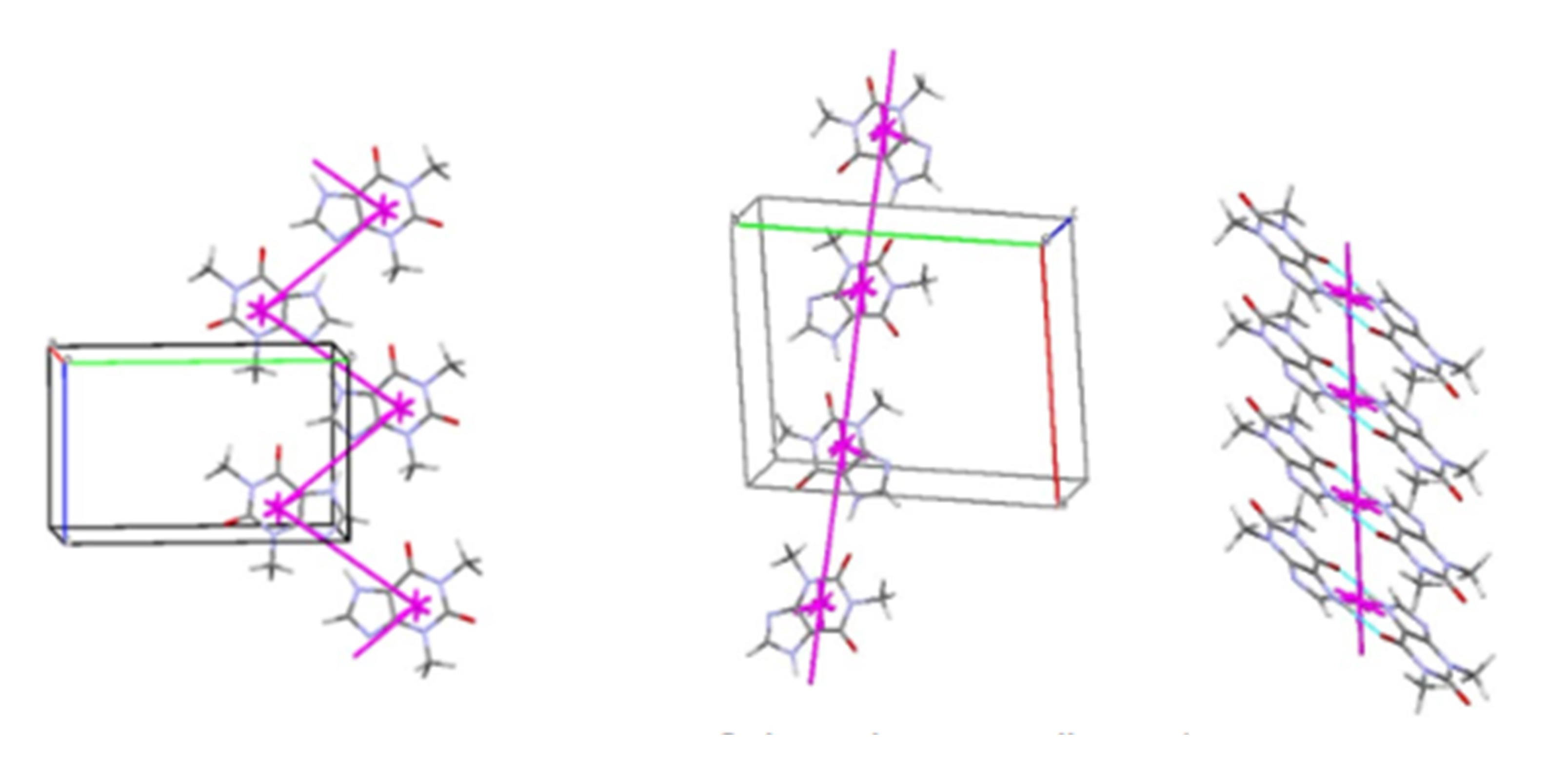
Діамінотриазоли, які є основною структурною одиницею для багатьох біологічно активних молекул, також демострують різноманітні способи кристалічної упаковки. Попри невеликий конформаційний простір, вони мають багато функціональних груп, здатних утворювати міжмолекулярні взаємодії різних типів. Дослідження двох поліморфних модифікацій диамінотриазолів показало різну будову кристалів з точки зору енергетичних векторних діаграм (Рис. 8, моноклінна модифікація – зліва та ромбічна – справа). Різниця між поліморфами обумовлена слабкими взаємодіями за участі аміногруп. Дослідження термічного розширення показали невелику різницю між поліморфними модифікаціями, а на основі енергій кристалічної гратки передбачено, що моноклінна модифікація має бути більш стабільною.
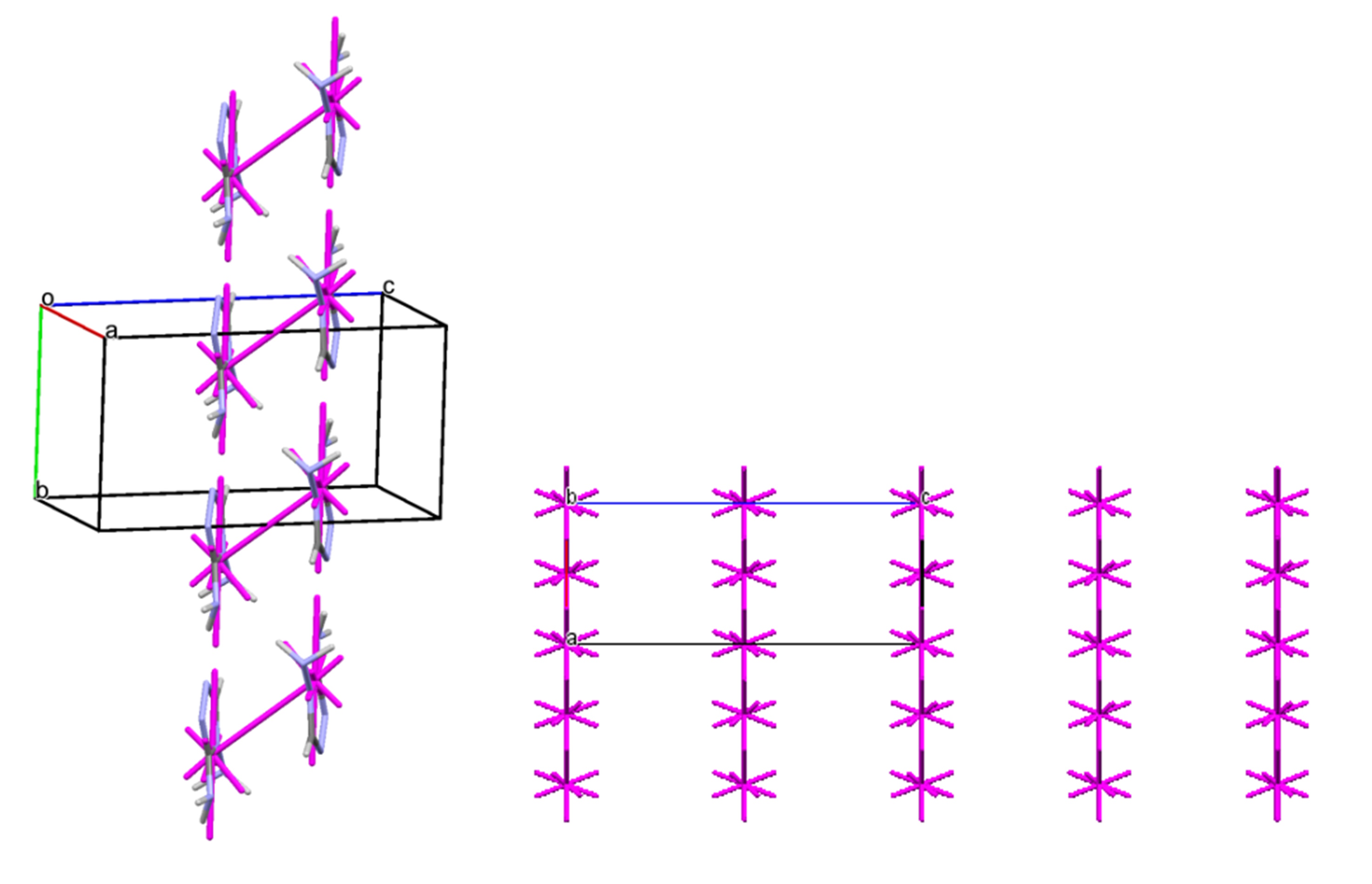
2. Аналіз кристалічних структур комплексоорганічних сполук
Комплексоорганічні сполуки мають велике значення для розвитку біологічної, фізичної та фармацевтичної хімії, і часто можуть бути отримані та вивчені лише у кристалічному стані. Вони проявляють велике різномаїття міжмолекулярних взаємодій, які призводять до різних способів упаковки молекул. У відділі проходили дослідження структур із лігандами на основі біологічно активного класу речовин – карбациламідофосфатів. Вони є аналогами b-дікетонів, втім проявляють відмінну від останніх поведінку під час координації.
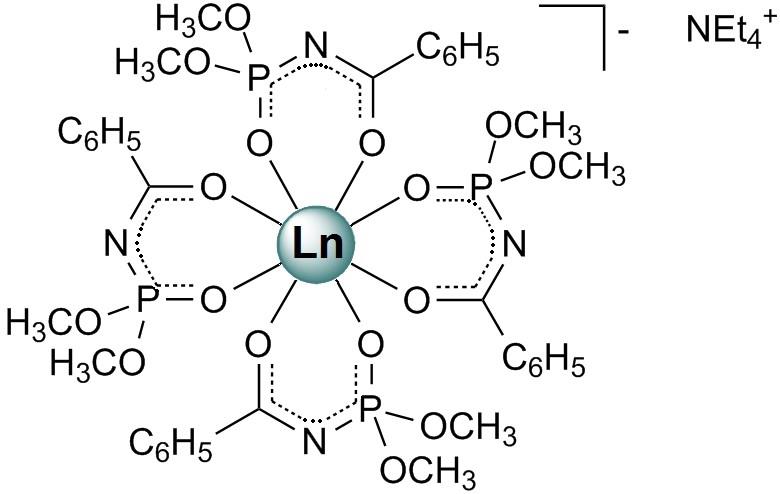
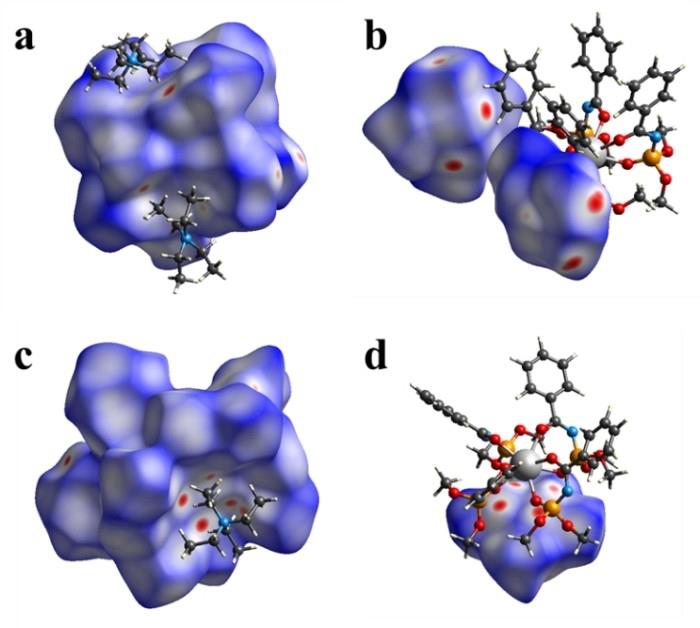
Досліджено структурні характеристики нових диметил-N- бензоїламідофосфатів (HL) на основі тетракіс-комплексів лантаноїдів NEt4[LnL4] (Ln3+ = Nd, Gd, Tb) (Рис. 9). Їхні координаційні поліедри схожі, втім самі структури демонструють різний спосіб кристалічної упаковки. Аналіз міжмолекулярних взаємодій з використанням анадізуі поверхні Хіршфельда показав домінуючу роль H…H контактів, тоді як внесок O…H/H…O, C…H/H…C є значно меншим (Рис. 10). Детальний аналіз міжмолекулярних взаємодій продемонстрував домінуючу роль нелокальних взаємодій, таких як стекінг та неспецифічні взаємодії, у формуванні кристалічної упаковки.
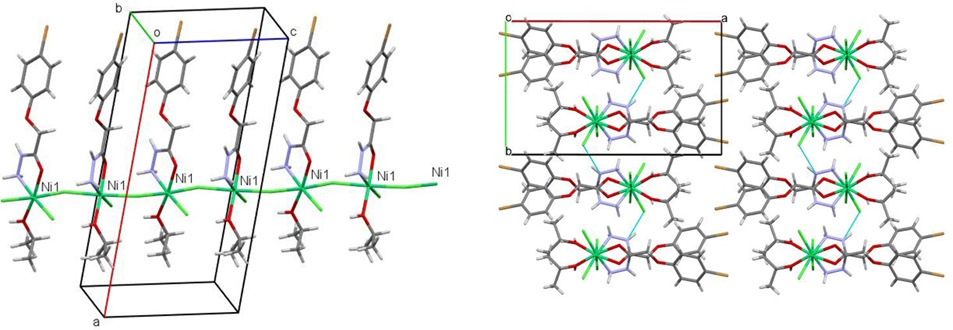
Іншим напрямком досліджень стали похідні гідразідів, які також є потенційними лікарськими препаратами. Було досліджено будову 2-(4-бромфенокси) ацетогідразиду та його комплексу з нікель(ІІ) хлоридом. У кристалічній фазі сполука утворює полімерні ланцюги за рахунок координаційних зв’язків, які зв’язуються у шари за допомогою вже слабших міжмолекулярних взаємодій (Рис. 11).
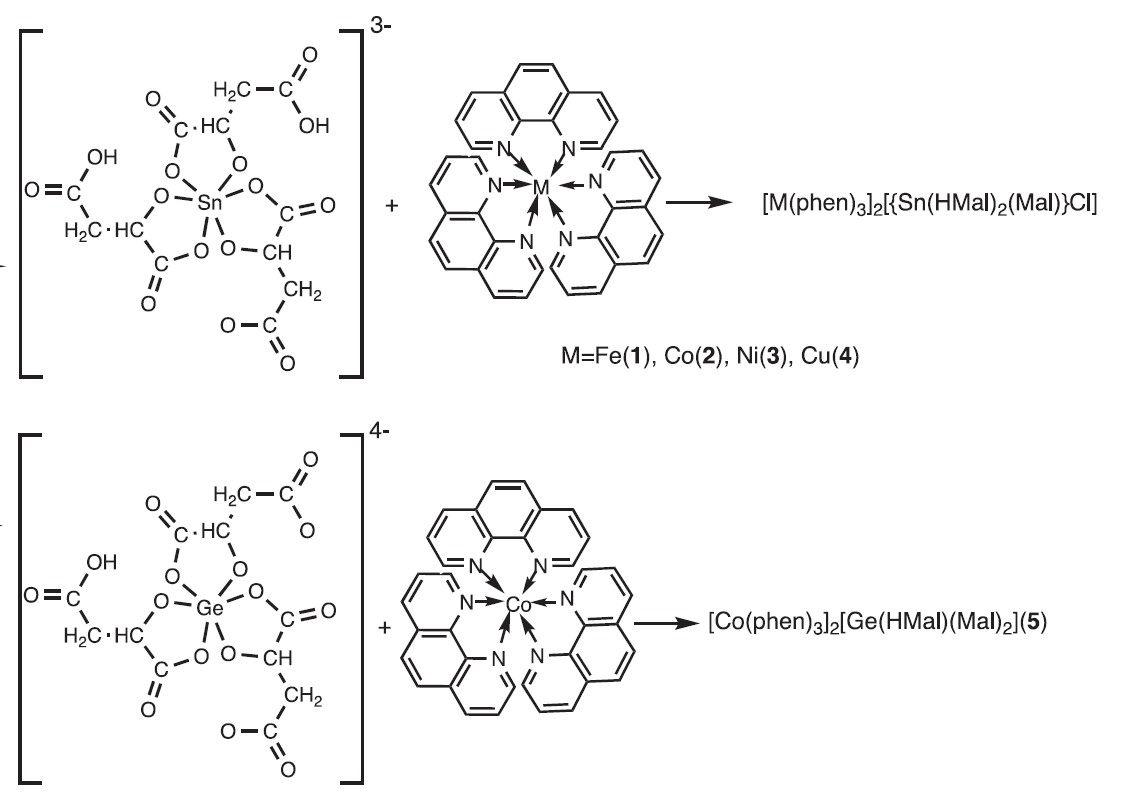
Також було вивчено будову та стереохімічні чинникі утворення 5 катіон-аніонних комплексів з подібними катіонами Fe(II), Co(II), Ni(II), Cu(II) 1,10-фенантроліну та різними комплементарними малато Ge/Sn-аніонами [M(phen)3]2[{Sn(HMal)2(Mal)}Cl] (M=Fe (2), Co (3), Ni (4), Cu (5)) та [Co(phen)3]2[{Sn(HMal)(Mal)2] (Рис. 12).
Проаналізовані міжмолекулярні зв’язки підтверджують ключовий внесок у формування поверхні Хіршвельда для всіх аніонів вносять зв'язки H...O/O...H, H...H, H...C/C...H та O...C/C...O, тоді як для катіонів більш важливу роль відіграють додаткові C...C взаємодії, що підтверджує наявність у їхніх структурах π-π-взаємодій.
3. Кристалічні структури ароматичних та неароматичних нітрогеновмісних сполук та їх відгуку на механічний тиск
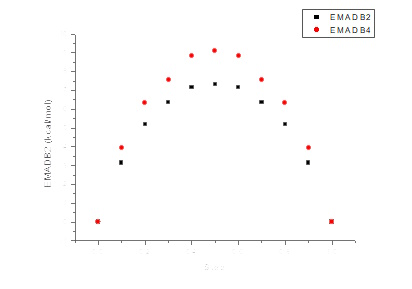
Проведено квантово-хімічне вивчення серії нітрогеновмісних сполук – похідних нітробензену, а також кон’югованих неароматичних нітрогеновмісних сполук, які демонструють вибухові властивості. Так, моделювання зміни структур ізомерних 2-аміно-1,3,-динітробензену МADB2 та 4-аміно-1,3-динітробензену MADB4, які структурно близькі до симм-триамінотринітробензену та мають шарувату кристалічну будову, виявило, що ізотропний механічний тиск до 20 ГПа призводить до зменшення довжин ортів елементарних комірок на 5 – 17%. MADB-2 та MADB-4 демонструють виражено анізотропний відгук, стискання відбувається переважно по напрямку, який співпадає з напрямком основного структурного мотиву – стекінгових колонок (що схоже на поведінку TATB). У MADB-2 він співпадає з напрямком орту (100), у MADB-4 стекінгові колонки розташовані вздовж напрямку (10-1), тому основне навантаження додаткового тиску беруть на себе параметри a та c.
Базові структурні мотиви в кристалах MADB-2 та MADB-4 під тиском змінюються послідовно: стовпчаста структура стає більш вираженою, оскільки стекінг-взаємодії втрачають в енергії менше, ніж інші типи взаємодій. Втім, принципового переходу не відбувається, що схоже на поведінку структури TATB.
Енергетичні профілі зсуву демонструють помірне значення енеретичного бар'єру деформації зсуву уздовж сусідніх шарів по шляху найменшого спротиву (Рис. 13).
Іншим напрямком є дослідження поліморфних модифікацій тринітротолуолу із метою виявити можливість переходу між ними під тиском. Базові структурні мотиви у ромбічній та моноклінній кристалічних модифікаціях сполуки є схожими і вирізняються невеликими відмінностями у другорядній організації структури, в той час як основою для обох є стекінгові стовпчики. Дослідження під впливом ізотропного тиску продемонструвало переважний механізму амортизації надлишкової енергії стискання за рахунок наближення шарів один до одного. Втім, на відміну від триамінотринітробензенів та моноамінодинітробензенів, у яких спостерігається схожа тенденція, у випадку TNT взаємодія між цими шарами не пов’язана зі стекінгом і є продуктом комбінації низки локальних і нелокальних міжмолекулярних парних взаємодій. Водночас на відміну від планарних нітроаміносполук, у випадку TNT максимальна амплітуда зміни параметрів комірки та анізотропія цих змін суттєво менша – що вказує на відсутність домінуючих взаємодій зі значними буферними властивостями на кшталт стекінгу.
Цікавими є результати порівняння поведінки кристалів ароматичних нітробензенів та неароматичного 1,1 - диаміно - 2,2 – динітроетилену (FOX7). FOX7 має кілька відомих поліморфні модифікацій, найстабільніші з яких мають шарувату структуру, причому моноклінна та ромбічна модифікації мають хвилясто-шарувату структуру, яка дуже подібна до структур розглянутих вище ізомерних диамінотринітробензенів (Рис. 14а-b), а от триклінна модифікація має планарно-шарувату структуру, яка подібна до симм-триамінотринітробензену (Рис. 15)
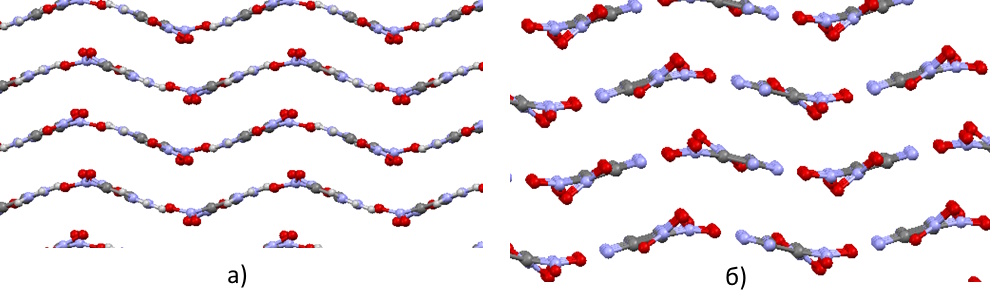
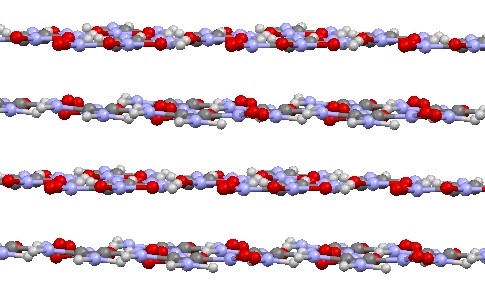
Збільшення тиску призводить до дещо різних наслідків для хвилясто-шаруватих та планарно-шаруватих структур, а також виявляє певні відмінності у поведінці ароматичних нітробензенів та неароматичного диамінодинітроетилену. Хоча основним шляхом компенсації механічного тиску для всіх вивчених структур залишається стискання у напрямку, перпендикулярному до площини шарів, хвилясто-шаруваті структури (ароматичні та неароматичні) виявляють помітну тенденцію до збільшення ступеню складчастості шарів. У неароматичному диамінодинітроетилені ця тенденція дещо сильніше виражена (крок хвилі зменшується на 14-16%, в той час як для ароматичних структур зменшення цього кроку досягає лише 9-13%). Планарні структури мають тенденцію до збереження планарних шарів. Втім, у неароматичній структурі триклінного диамінодинітроетилену зафіксовано суттєво більша ступень молекулярної деформації під тиском (максимальні кути розвороту нітрогруп від площині молекули досягають 36° за тиску 20 ГПа, в той час як молекула ТАТВ зберігає планарну структуру з максимальними кутами розвороту нітрогруп до 15°).
4. Вивчення процесів фазових переходів та гідратації/дегідратації неорганічних речовин методами порошкового рентгеноструктурного аналізу
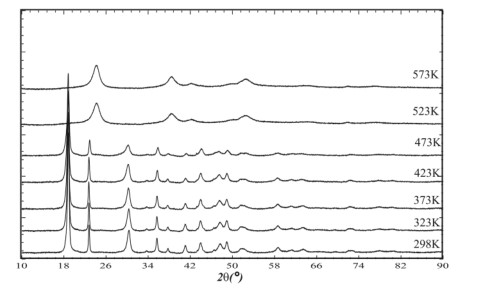
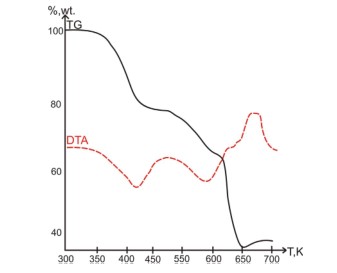
Термічне розкладання дигідрату оксалату нікелю зрештою приводить до розупорядкованої кристалічної форми безводного карбонату нікелю. Порошкові діфрактограми сполуки у процесі розкладання дають змогу побудувати діаграми дегідратації та визначити головні кроки перетворення сполуки у твердому стані (Рис. 16 - 17).
5. Дослідження лікарських препаратів
У співробітництві з фармацевтичними компаніями України постійно виконуються рентгеноструктурні вимірювання зразків комерційних лікарських препаратів для визначення фазового складу речовин.